Управление рисками в клинических исследованиях
Какие риски возникают при проведении клинического исследования? Как происходит идентификация и управление рисками? Что такое план управления рисками в клинических исследованиях? В сегодняшней статье мы разберём данные вопросы и расскажем о процессах управления рисками в клинических исследованиях.
Для начала разделим возможные риски на группы, соответствующие этапам КИ:
- Получение одобрения регуляторных органов
- Задержка в получении одобрения исследования ЛЭКом;
- Задержка в получении одобрения исследования Минздравом РФ;
- Запуск КИ
- Задержка с подписанием контракта с центром;
- Задержка введения полученных первичных данных (включая оборот запросов на уточнение информации) исследовательским центром;
- Отклонение сроков открытия центра;
- Набор пациентов / здоровых добровольцев
- Низкая (ниже запланированной) скорость набора субъектов;
- Риск включения добровольцев в исследование (рандомизация) с несоблюдением критериев включения/невключения;
- Проведение КИ
- Остановка производства исследуемого препарата (ИП)/закупка препарата сравнения;
- Риск, связанный с невозможностью выполнения условий договора аналитической лабораторией/центральной лабораторией;
- Невозможность маркировки ИП/ПС согласно требованиям надлежащей производственной практики;
- Остановка очного мониторирования исследования исследовательских центров;
- Проблемы с качеством данных (ведение первичной документации, ошибки переноса данных из первичной документации в ИРК, ошибки ведения журналов исследовательского центра и исследования);
- Несоблюдение требований протокола;
- Риск задержки верификации данных;
- Подготовка финального отчёта
- Искажение структуры и содержания отчёта;
- Отсутствие индивидуальных перечней отклонений, лабораторных показателей, НЯ;
- Отклонения от плана статистического анализа (которые не зафиксированы в разделе «Отклонения от протокола и стат. анализа);
- Не приведены нормы лабораторных и физикальных показателей;
Перечисленные риски оказывают разное влияние на выполнение проекта и имеют разную вероятность возникновения.
Рассмотрим подробнее процесс управления рисками в клинических исследованиях. Управление рисками — это процесс, связанный с идентификацией, анализом рисков и принятием решений, направленные на максимизацию положительных и минимизацию отрицательных последствий наступления рисковых событий.
Процесс управления рисками состоит из следующих этапов:
Идентификация риска — это систематическое использование информации для выявления опасности в отношении аспекта риска или же для описания проблемы.
Оценка риска — это процесс понимания природы риска и определения уровня риска.
Принятие решений по риску — это действие по принятию решения по снижению/устранению или принятию риска. По результатам оформляют протокол корректирующих и предупреждающих действий, определяя необходимый уровень контроля выполнения.
Информирование о риске — это обмен информацией по рискам и управлением рисками и управлением рисками между лицами, принимающими решение, сотрудниками компании на любом этапе процесса управления рисками. При выявлении рисков важно проинформировать заинтересованные стороны и руководство. Это должно быть закреплено соответствующими СОП компании.
Мониторинг риска — неотъемлемая часть процесса управления рисками. Для этого необходимо формировать отчёты о проектных рисках как части регулярного отчета о ходе выполнения проекта. Частота отчётов должна быть обоснована риском. На этом этапе целесообразно оценить эффективность проведения мероприятий по устранению/снижению риска.
Оценка рисков фиксируется в плане управления рисками. Цель плана управления рисками в клиническом исследовании заключается в обеспечении единой терминологии по рискам, а также в поддержке проактивного выявления, оценки, контроля, обзора, информирования и отчетности по рискам на протяжении всего жизненного цикла проекта.
В плане управления рисками описывается, каким образом будут осуществляться, регистрироваться и контролироваться мероприятия по управлению рисками на протяжении всего жизненного цикла проекта. План управления рисками разрабатывается для того, чтобы обеспечить надлежащее управление любыми потенциальными угрозами реализации проекта и минимизации рисков срыва проекта.
План управления рисками состоит из следующих разделов:
- Распределение обязанностей между Спонсором исследования и контрактной исследовательской организации.
- Матрица оценки рисков – бланк, который обеспечивает качественный анализ уровня риска, реализации нежелательного события во время реализации проекта. Визуально представляет из себя двухмерную матрицу, в которой вероятность возникновения риска растет по оси X, а степень влияния риска возрастает по участку оси Y.
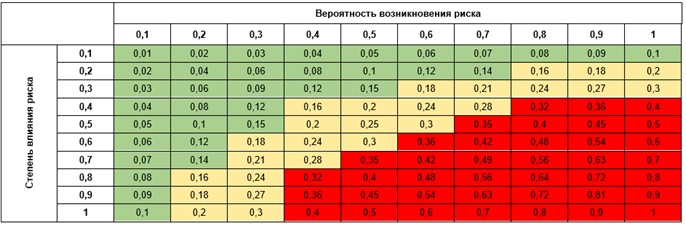
- Базовая оценка рисков. В таблице перечислены потенциальные риски проекта. Риски подразделяются на группы, относящиеся к разным сторонам проекта: спонсору исследования, контрактной исследовательской организации, клиническому центру. Каждому риску присваивается вероятность возникновения, степень влияния на выполнение проекта и результирующий показатель согласно Матрице оценки рисков. Затем предлагаются действия по снижению влияния указанных рисков.
В заключении стоит подчеркнуть, что Спонсор клинического исследования в соответствии с правилами надлежащей клинической практики должен обеспечивать качественное проведение клинических исследований. Необходимо комплексно подходить к устранению/снижению рисков, осуществляя регулярный контроль ситуации независимо от стадии проведения находится клиническое исследование.



