Китайский регулятор отклонил 542 заявки на лекарственные препараты в 2021 году
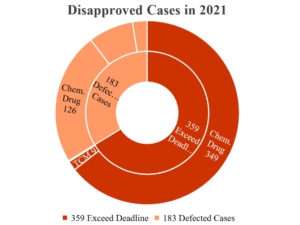
В 2021 году Китайский центр по оценке заболеваний (China’s Center for Disease Evaluation, CDE) отклонил 542 заявки на регистрацию лекарственных средств. Из них 359 были отклонены по причине несвоевременного предоставления дополнительных досье (далее «Превышение срока»), что составляет 66,3% от всех отклоненных заявок. К просроченным относятся заявки 9 препаратов традиционной китайской медицины (ТКМ), 349 химических препаратов и 1 биологического препарата.
Остальные 183 заявки (далее «Дефектные случаи») были отклонены по причинам, связанным с безопасностью, эффективностью, качеством и другими, включая 14 препаратов ТКМ, 126 химических препаратов и 43 биологических продукта (см. следующую диаграмму):
I. Основные проблемы, выявленные китайским регулятором:
- Недостаточная информация и вопросы выполнимости (Feasibility)
Эта проблема существует в основном на ранней стадии разработки лекарств, некоторых дженериков, в основном, в следующих аспектах:
- Неясная клиническая позиция исследований и разработки лекарств;
- Необоснованный выбор индикаторов;
- Необоснованный выбор лекарственной формы или способа введения;
- Неэффективность препарата, предполагаемая на основе существующих данных исследований;
- Неоднозначная цель, механизм действия и т.д.
- Эффективность лекарств
- Представленные данные КИ не демонстрируют эффективность препарата;
- Проблемы, связанные с протоколом КИ или контролем качества исследования, приводящие к признанию недействительными показаний к применению исследуемого препарата;
- Результаты исследований биоэквивалентности препарата-дженерика не показали эквивалентности референтному лекарственному препарату;
- Отсутствие клинических данных для китайской этнической группы.
- Безопасность лекарств
- Результаты ранней фазы предполагают, что токсичность значительна, или риски для безопасности слишком высоки, чтобы оправдать дальнейшие разработки;
- Проблемы с методами доклинического исследования безопасности или проблемы контроля качества исследования, или недостаточное количество данных исследования для поддержки последующей разработки;
- Имеющиеся данные клинических исследований свидетельствуют о серьезных нежелательных реакциях, а соотношение «польза-риск» является необоснованным;
- Отсутствие клинических данных по безопасности в китайских этнических группах.
- Контроль качества
- Несоответствие качества референтного лекарственного препарата;
- Несоответствие исследуемых образцов на каждом этапе разработки;
- Несоблюдение китайских технических требований к маркетингу в отношении дженериков;
- Неиспользование фармацевтических субстанций законного происхождения в соответствии с требованиями;
- Несоответствие тестируемых образцов китайским правилам.
- Соблюдение нормативных требований
Существенной причиной отклонения заявки на ЛП являются пробелы в нормативной базе и несоответствие требованиям Национального управления медицинской продукции Китая (NMPA), включая, но не ограничиваясь следующими тремя аспектами:
- Пробелы в данных в соответствии с китайскими требованиями;
- Серьезные дефекты, влияющие на качество продукции;
- Дисквалификация в ходе выборочной проверки.
- Прочие проблемы
- Непредоставление необходимых данных или дополнительных материалов по запросу Китайского центра по оценке заболеваний;
- Отсутствие необходимых данных, обнаруженное во время технической экспертизы.
II. Предложения:
- Соблюдение нормативных требований Китая
- Крайне важно своевременно предоставлять все требуемые материалы и соблюдать сроки;
- Рекомендуется проводить тщательную оценку соответствия нормативным требованиям и анализ пробелов в досье, чтобы свести к минимуму вероятность отклонения заявки.
- Внимание к основам разработки лекарств
- Разработка и регистрация лекарственных препаратов должны основываться на потребностях и размере китайского рынка;
- На первое место должна быть поставлена клиническая ценность. Необходимо уделять внимание преимуществам разработки аналогичных инновационных препаратов
Источник: Accestra Consulting Company, www.accestra.com